Los hidróxidos resultan de la combinación entre un óxido metálico (también llamados óxidos básicos) y el agua. De esta forma, la composición de los hidróxidos viene dada por tres elementos: el oxígeno, el hidrógeno y el metal en cuestión. En la combinación, el metal siempre actúa como catión y el grupo hidróxido (OH–) actúa como anión. Por ejemplo:
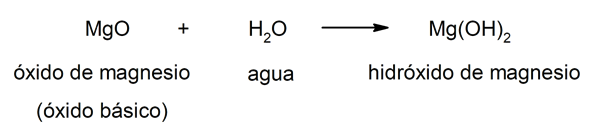
Los hidróxidos, en general, comparten una serie de características, como presentar un sabor amargo y ser cáusticos. Además, suelen ser resbaladizos al tacto y corrosivos. Por otra parte, poseen algunas propiedades de los detergentes y jabones. La mayoría son solubles en agua y reaccionan con los ácidos para producir sales.
Algunas características, en cambio, son propias de cada tipo de hidróxido, como el de sodio (NaOH), que absorbe agua, y mezclado con cal viva (CaO) absorbe rápidamente dióxido de carbono (CO2). Por su parte, el hidróxido de calcio (Ca(OH)2) se obtiene en la reacción del óxido de calcio con el agua y también absorbe el CO2. Otro ejemplo es el hidróxido de hierro (II) (Fe(OH)2), que es un compuesto gelatinoso y prácticamente es insoluble en el agua.
A los hidróxidos también se les llama bases o álcalis, aunque estos términos se han ido ampliando también para otras sustancias con carácter alcalino y que no son hidróxidos.
Puede servirte: Óxidos ácidos
¿Para qué se utilizan los hidróxidos?
Las aplicaciones de los hidróxidos también varían entre los diferentes casos:
- El hidróxido de sodio, por ejemplo, se asocia a la industria de los jabones y los productos de belleza y cuidado corporal.
- El hidróxido de calcio, por su parte, tiene un papel intermediario en algunos procesos como el de la obtención del carbonato sódico (Na2CO3).
- El hidróxido de litio (LiOH) se usa en la fabricación de cerámica, mientras que el de magnesio (Mg(OH)2) se usa como antiácido o como laxante.
- El hidróxido de hierro se utiliza en el proceso de fertilización de plantas.
Nomenclaturas de los hidróxidos
Al igual que para nombrar otros tipos de compuestos químicos, existen diferentes nomenclaturas para los hidróxidos:
- Nomenclatura tradicional. Se nombran poniendo la palabra “hidróxido” seguido del nombre del metal precedido o terminado en un determinado prefijo o sufijo que depende de la cantidad de estados de oxidación que tenga:
- Si el metal tiene solo un estado de oxidación, se le pone a su nombre el sufijo ‘ico’. Por ejemplo: hidróxido sódico/Na(OH).
- Si el metal tiene dos estados de oxidación, se le pone a su nombre el sufijo ‘ico’ cuando tiene el mayor y el sufijo ‘oso’ cuando tiene el menor. Por ejemplo: hidróxido ferroso (II)/Fe(OH)2 e hidróxido férrico/Fe(OH)3.
- Si el metal tiene tres estados de oxidación, se le pone a su nombre el prefijo ‘hipo’ y el sufijo ‘oso’ cuando tiene el menor, el sufijo ‘oso’ para el que sigue y el sufijo ‘ico’ cuando tiene el mayor. Por ejemplo: hidróxido hipocromoso/Cr(OH)2, hidróxido cromoso/Cr(OH)3 e hidróxido crómico/Cr(OH)6.
- Si el metal tiene cuatro estados de oxidación, se le pone a su nombre el prefijo ‘hipo’ y el sufijo ‘oso’ cuando tiene el menor, el sufijo ‘oso’ para el que sigue, el sufijo ‘ico’ para el siguiente y el prefijo ‘per’ y el sufijo ‘ico’ cuando tiene el mayor. Por ejemplo: hidróxido hipovanadoso/V(OH)2, hidróxido vanadoso/V(OH)3, hidróxido vanádico/V(OH)4 e hidróxido pervanádico/V(OH)5.
- La nomenclatura de Stock. Utiliza la palabra hidróxido, pero en vez de complementar con una sola palabra, usa la preposición ‘de’ y luego el nombre del metal, colocando entre paréntesis la valencia correspondiente a cada compuesto. Por ejemplo: hidróxido de hierro (II)/Fe(OH)2 e hidróxido de hierro (III)/Fe(OH)3.
- La nomenclatura sistemática. Se nombran anteponiendo los prefijos numéricos a la palabra ‘hidróxido’. Por ejemplo: dihidróxido de hierro/Fe(OH)2 y trihidróxido de hierro/Fe(OH)3.
Ejemplos de hidróxidos
- Hidróxido de plomo (II), Pb(OH)2, dihidróxido de plomo.
- Hidróxido de platino (IV), Pt(OH)4, tetrahidróxido de platino.
- Hidróxido vanádico, V(OH)4, tetrahidróxido de vanadio.
- Hidróxido ferroso, Fe(OH)2, dihidróxido de hierro.
- Hidróxido de plomo (IV), Pb(OH)4, tetrahidróxido de plomo.
- Hidróxido de plata, AgOH, hidróxido de plata.
- Hidróxido de cobalto, Co(OH)2, dihidróxido de cobalto.
- Hidróxido de manganeso, Mn(OH)3, trihidróxido de manganeso.
- Hidróxido férrico, Fe(OH)3, trihidróxido de hierro.
- Hidróxido cúprico, Cu(OH)2, dihidróxido de cobre.
- Hidróxido de aluminio, Al(OH)3, trihidróxido de aluminio.
- Hidróxido de sodio, NaOH, hidróxido de sodio.
- Hidróxido de estroncio, Sr(OH)2, dihidróxido de estroncio.
- Hidróxido de magnesio, Mg(OH)2, dihidróxido de magnesio.
- Hidróxido de amonio, NH4OH, hidróxido de amonio.
- Hidróxido de cadmio, Cd(OH)2, dihidróxido de cadmio.
- Hidróxido vanadoso, V(OH)3, trihidróxido de vanadio.
- Hidróxido mercúrico, Hg(OH)2, dihidróxido de mercurio.
- Hidróxido cuproso, CuOH, hidróxido de cobre.
- Hidróxido de litio, LiOH, hidróxido de litio.
En ocasiones, los hidróxidos tienen nombres comunes dados por sus usos más convencionales: el hidróxido de sodio también se denomina soda cáustica, el hidróxido de potasio se denomina potasa cáustica, el hidróxido de calcio que se denominada agua de cal o cal apagada y el hidróxido de magnesio que se denomina leche de magnesia.
Sigue con:
¿Te fue útil esta información?
Sí No¡Genial! gracias por visitarnos :)